Bộ 30 đề thi học kì 1 Hóa 11 có đáp án (Đề 17)
27 người thi tuần này 4.6 18.1 K lượt thi 24 câu hỏi 45 phút
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
🔥 Học sinh cũng đã học
Trắc nghiệm Ôn tập chương 6 lớp 11 (có đáp án - phần 2)
Trắc nghiệm Carboxylic acid lớp 11 (có đáp án - phần 2)
Trắc nghiệm Hợp chất carbonyl lớp 11 (có đáp án - phần 2)
Trắc nghiệm Ôn tập chương 5 lớp 11 (có đáp án - phần 2)
Bài tập về phản ứng tách nước tạo alkne của alcohol lớp 11 (có lời giải)
Danh sách câu hỏi:
Câu 1/24
A. 0,03.
B. 0,10.
C. 0,01.
D. 0,30.
Lời giải
Chọn đáp án D
Phương pháp giải:
Tính theo PTHH: 3NaOH + H3PO4 → Na3PO4 + 3H2O
Giải chi tiết:
PTHH : 3NaOH + H3PO4 → Na3PO4 + 3H2O
0,009 ← 0,003 0,003 mol
→ CM = n : V → a = 0,009 : 0,03 = 0,3M
Câu 2/24
A. 53,2 gam
B. 40,8 gam
C. 39,7 gam
D. 37,4 gam
Lời giải
Chọn đáp án B
Phương pháp giải:
Bảo toàn điện tích: 2nCa2+ + 2nBa2+ = nCl– + nHCO3– → a
Khi đun nóng X: 2HCO3– CO32– + H2O + CO2
→ nHCO3– = ½.a → mmuối = mCa2+ + mBa2+ + mCl– + mCO32–
Giải chi tiết:
Bảo toàn điện tích: 2nCa2+ + 2nBa2+ = nCl– + nHCO3– → 0,2.2 + 0,1.2 = 0,2.1 + a → a = 0,4 mol
Khi đun nóng X: 2HCO3– CO32– + H2O + CO2
→ nCO3– = ½.a = 0,2 mol
Ta có: mmuối = mCa2+ + mBa2+ + mCl– + mCO32– = 0,2.40 + 0,1.137 + 0,2.35,5 + 0,2.60 = 40,8 gam
Câu 3/24
A. C + O2 CO2.
B. C + 2H2 CH4.
C. 3C + CaO CaC2 + CO
D. 3C + 4Al Al4C3.
Lời giải
Chọn đáp án A
Phương pháp giải:
Tính khử là khả năng nhường electron của chất, chất đó sẽ tăng số oxi hóa.
Giải chi tiết:
A. Cacbon tăng số oxi hóa C0 lên C+4 → tính khử
B. Cacbon giảm số oxi hóa từ 0 xuống – 4 → tính oxi hóa
C. Cacbon giảm số oxi hóa từ 0 xuống –1 (CaC2) và cả số oxi hóa tăng từ 0 lên +2 (CO) → cả tính khử và oxi hóa
D. Cacbon giảm số oxi hóa từ 0 xuống –4 → tính oxi hóa
Câu 4/24
A. N2O.
B. NO2.
C. N2.
D. NO.
Lời giải
Chọn đáp án C
Phương pháp giải:
Giả sử 1 mol khí trao đổi n mol electron.
Áp dụng bảo toàn e: 2nMg = n.n khí → Giá trị của n
+ n = 1 → NO2
+ n = 3 → NO
+ n = 8 → N2O
+ n = 10 → N2
Giải chi tiết:
nMg = 0,1 mol và nX = 0,02 mol
Giả sử 1 mol khí trao đổi n mol electron
Áp dụng bảo toàn e: 2nMg = n.n khí → 2.0,1 = 0,02.n → n = 10
→ Khí là N2
Câu 5/24
A. V2 = 2V1.
B. 2V2 = V1.
C. V2 = V1.
D. 3V2 = 2V1.
Lời giải
Chọn đáp án A
Phương pháp giải:
3Cu + 8H++ 2NO3– → 3Cu2+ + 2NO + 4 H2O (1)
TN1: V1 lít
TN2: 3V1 lít
Nhận thấy: nH+ (TN2) = 3nH+ (TN1) → Thí nghiệm 2 có H2SO4 và HNO3 trong khí thí nghiệm 1 chỉ có HNO3
→ (1) là HNO3; (2) là NaNO3; (3) là H2SO4
Sau đó dựa vào PT (1) để tính nNO thoát ra ở các thí nghiệm 1 và 3. Từ đó suy ra V2 và V1
Giải chi tiết:
3Cu+ 8H++ 2NO3– → 3Cu2++ 2NO + 4 H2O
TN1: V1 lít
TN2: 2V1 lít
Nhận thấy: nH+ (TN2)= 2nH+ (TN1) → Thí nghiệm 2 có H2SO4 trong khí thí nghiệm 1 chỉ có HNO3
→ (1) là NaNO3; (2) là HNO3; (3) là H2SO4
Ta có: TN1 thì nH+ = 5.10–3 mol và NO3–: 10.10–3 mol
TN2 thì nH+= 10.10–3 mol và NO3–: 5.10–3 mol
3Cu+ 8H+ + 2NO3– → 3Cu2++ 2NO + 4 H2O
TN1: Bđ: 5.10–3 10.10–3
Pư: 5.10–3→ 1,25.10–3
TN3: Bđ: 10.10–3 5.10–3
Pư: 10.10–3 → 2,5.10–3
Các thể tích khí đo ở cùng điều kiện nên nNO(TN3) = 2nNO (TN1) → VNO(TN3) = 2VNO (TN1) hay V2 = 2V1
Câu 6/24
A. Dung dịch KNO3.
B. Dung dịch NaCl.
C. Dung dịch NaOH.
D. Dung dịch KCl.
Lời giải
Chọn đáp án C
Trong điều kiện thường Si tan được trong dung dịch NaOH:
2NaOH + Si + H2O → Na2SiO3 + 2H2
Câu 7/24
A. 0,345 gam.
B. 0,690 gam.
C. 0,460 gam.
D. 0,920 gam.
Lời giải
Chọn đáp án C
Phương pháp giải:
Đặt số mol của Na và Ca trong X lần lượt là x và y mol
Bảo toàn Na có nNaOH = x mol
Bảo toàn Ca có nCa(OH)2 = y mol → nOH– = x + 2y (mol)
Khi sục CO2 vào thì kết tủa max khi nCa2+ = nCaCO3 → y
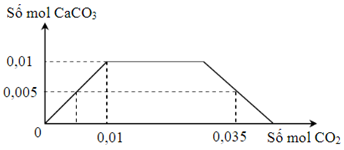
Xét thời điểm nCO2 = 0,035 mol thì xảy ra cả phản ứng tạo CO32– và HCO3–
CO2 + 2OH– → CO32– + H2O
CO2 + OH– → HCO3–
Ca2+ + CO32– → CaCO3
Ta có nCO32– = nCaCO3
Bảo toàn C có nHCO3– = nCO2 – nCO32– → nOH– phản ứng = 2nCO32– + nHCO3– → x + 2y → x
Giải chi tiết:
Đặt số mol của Na và Ca trong X lần lượt là x và y mol
Bảo toàn Na có nNaOH = x mol
Bảo toàn Ca có nCa(OH)2 = y mol
→ nOH– = x + 2y (mol)
Khi sục CO2 vào thì kết tủa max khi nCa2+ = nCaCO3 = 0,01 mol = y
Xét thời điểm nCO2 = 0,035 mol thì xảy ra cả phản ứng tạo CO32– và HCO3–
CO2 + 2OH– → CO32– + H2O
CO2 + OH– → HCO3–
Ca2+ + CO32– → CaCO3
Ta có nCO32– = nCaCO3 = 0,005 mol
Bảo toàn C có nHCO3– = nCO2 – nCO32– = 0,035 – 0,005 = 0,03 mol
→ nOH– phản ứng = 2nCO32– + nHCO3– = 2.0,005 + 0,03 = 0,04 mol
→ x + 2y = 0,04 → x = 0,04 – 2y = 0,02 mol ( y = 0,01 mol) → mNa = 0,02.23 = 0,46 gam
Lời giải
Chọn đáp án B
Phương pháp giải:
Chất điện li là axit, bazơ và hầu hết các muối.
Giải chi tiết:
Chất điện li ở dây là NaCl (muối ăn) – natri clorua.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 10/24
A. CuO, NO2, O2.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 11/24
A. cacbon.
B. kali.
C. nitơ.
D. photpho.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 13/24
A. đỏ
B. trắng
C. xanh
D. vàng
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 14/24
A. 0,5.
B. 2,0.
C. 0,2.
D. 1,0.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 15/24
A. K+ + H+ → KH.
B. K+ + Cl– → KCl.
C. H+ + OH– → H2O.
D. OH– + Cl– → HClO.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 18/24
A. Ba2+, Mg2+, PO43–, SO4 2–.
B. H+, Al3+, OH–, NO3–.
C. K+, Na+, SO42–, NO3–.
D. Ba2+, Mg2+, Cl–, CO32–.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 20/24
A. NH4Cl HCl + NH3.
B. 2NH4Cl + Ca(OH)2 → CaCl2 + 2NH3 + 2H2O.
C. N2 + 3H2 2NH3.
D. NH4HCO3 NH3 + CO2 + H2O.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Xem tiếp với tài khoản VIP
Còn 16/24 câu hỏi, đáp án và lời giải chi tiết.
Bạn cần đăng ký gói VIP ( giá chỉ từ 250K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.