Đề thi thử tốt nghiệp THPT môn Hóa Cụm Đô Lương - Yên Thành 3 - Nghệ An năm 2025 có đáp án
89 người thi tuần này 4.6 2.3 K lượt thi 40 câu hỏi 60 phút
🔥 Đề thi HOT:
Đề thi thử THPTQG 2019 môn Hóa học cực hay có lời giải chi tiết (P1)
Đề Ôn thi THPTQG 2019 Hóa Học cơ bản, nâng cao có lời giải chi tiết (P1)
Tổng hợp đề thi Thử Hóa học cực hay có lời giải (Đề số 1)
Đề thi thử Hóa học cực hay có lời giải chi tiết (đề số 1)
Tổng hợp minh họa THPTQG 2019 Hóa Học có lời giải (Đề số 1)
Tổng hợp đề thi thử THPTQG 2019 - chuẩn cấu trúc của bộ giáo dục (Đề số 1)
Bộ đề tăng tốc luyện thi Hóa Học cực hay có lời giải chi tiết (đề số 1)
15 Đề thi thử THPTQG 2019 Hóa Học chuẩn cấu trúc của bộ giáo dục (Đề số 1)
Nội dung liên quan:
Danh sách câu hỏi:
Lời giải
A
Ở trạng thái cơ bản, cấu hình electron của nguyên tử K (Z = 19) là: [Ar] 4s1. (Khí hiếm Ar có Z = 18)
Lời giải
C
(a) Sai, cao su tự nhiên được lấy từ cây cao su.
(b) Đúng
(c) Đúng, các mạch không nhánh được khâu lại thành mạch polymer bằng các cầu nối -S-S-
(d) Sai, phản ứng cộng HCl vào C=C không làm thay đổi mạch polymer.
Câu 3
Lời giải
B
Cặp có thế điện cực chuẩn lớn nhất kết hợp với cặp có thế điện cực chuẩn nhỏ nhất sẽ được pin có sức điện động chuẩn lớn nhất.
→ Pin có E° lớn nhất là Al-Ag (E° = 0,80 – (-1,68) = 2,48V)
Câu 4
Lời giải
D
Trùng hợp CH2=CH–CH3 thu được polypropylene:
nCH2=CH–CH3 → [-CH2-CH(CH3)-]n
Câu 5
Lời giải
A
Nguyên tắc tách kim loại ra khỏi hợp chất của chúng là khử ion kim loại trong hợp chất thành nguyên tử:
Mn+ + ne → M
Câu 6
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 199K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 7
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 199K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 8
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 199K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 9
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 199K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 10
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 199K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 11
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 199K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 12
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 199K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 13
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 199K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 14
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 199K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 15
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 199K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 16
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 199K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 17
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 199K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 18
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 199K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 199K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 199K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 199K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 199K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 199K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 199K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Đoạn văn 1
PHẦN II. Câu trắc nghiệm đúng sai. Thí sinh trả lời từ câu 19 đến câu 22. Trong mỗi ý a), b), c), d) ở mỗi câu, thi sinh chọn đúng hoặc sai.
Aspirin (hay acetylsalicylic acid), là một dẫn xuất của salisylic acid được sử dụng để hạ sốt và giảm đau nhẹ đến trung bình do tình trạng đau nhức cơ, răng, cảm lạnh đau đầu và sưng tấy do viêm khớp. Một nhóm học sinh thực hiện tổng hợp Aspirin trong phòng thí nghiệm như sau:
Bước 1: Cho 75,0 gam salicylic acid khan và 105,0 ml acetic nhydride (d = 1,08 g/mL) vào bình cầu 250 ml; thêm 4,0 ml sulfuric acid đặc vào và lắc kĩ. Sau đó, khuấy khối phản ứng ở 50 – 60°C trong khoảng 45 phút cho đến khi tan hết phần chất rắn.
Bước 2: Dùng nước đá để làm lạnh hỗn hợp phản ứng đến nhiệt độ nhỏ hơn 10°C. Cho hỗn hợp vào cốc lớn, thêm từ từ 750 ml nước cất và khuấy kỹ, aspirin sẽ kết tủa. Lọc lấy sản phẩm bằng phễu lọc Buchner.
Bước 3: Hòa tan aspirin thô trong 100 ml ethanol 90°, đun nóng để tan hoàn toàn, sau đó đổ dung dịch này từ từ vào 450 ml nước nóng khoảng 50°C, đun nóng nhẹ cho chất rắn tan hết. Để nguội dung dịch thu được đến nhiệt độ phòng. Aspirin kết tinh dưới dạng tinh thể, lọc và hút hết nước, sây khô ở 50°C.
Bước 4: Cân sản phẩm thu được 83,1 gam aspirin.
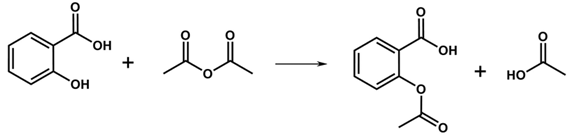
Biết phương trình hóa học điều chế aspirin từ salicylic acid được biểu diễn như sau:
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 199K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 199K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 199K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 199K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Đoạn văn 2
Một nhóm học sinh tiến hành mạ đồng (copper) cho một chiếc chìa khóa bằng hợp kim Fe-Zn, quá trình tiến hành được thực hiện như sau:
- Cho vào cốc thủy tinh 200 mL dung dịch CuSO4 1 M.
- Nhúng 1 lá đồng vào dung dịch và nối với cực dương của nguồn điện 1 chiều.
- Nhúng chìa khóa chìm trong dung dịch và nối với cực âm của nguồn điện.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 199K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 199K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 199K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 199K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Đoạn văn 3
Một nhóm học sinh tiến hành dự án nấu rượu truyền thống bằng cách lên men tinh bột, nhằm kiểm tra giả thuyết "sau khi thủy phân, lên men, chưng cất sẽ thu được rượu chỉ chứa C2H5OH và H2O”, sau đó đem bán lấy kinh phí góp thực hiện chương trình "Xuân yêu thương". Tinh bột từ gạo nếp sau khi nấu cơm, ủ lên men, thêm nước đủ ngày, sau đó chưng cất thu được rượu 30°. Trong quá trình chưng cất, chất lỏng ban đầu thu được có vị rất nồng, sau đó nhạt dần và cuối cùng có vị chua.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 199K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 199K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 199K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 199K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Đoạn văn 4
Tiến hành thí nghiệm theo các bước sau:
Bước 1: Cho vào 3 ống nghiệm, mỗi ống 2 mL dung dịch H2SO4 0,5 M.
Bước 2: Cho 3 lá kim loại có kích thước như nhau đã làm sạch lớp bề mặt gồm lá Zn (Zinc) vào ống nghiệm (1), lá Fe (Iron) vào ống nghiệm (2) và lá Mg (Magnesium) vào ống nghiệm (3). Biết: E°Zn2+/Zn = -0,762V, E°Fe2+/Fe = -0,44V; E°Mg2+/Mg = -2,356V; E°Cu2+/Cu = +0,34V và E°2H+/H2 = 0,0V.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 199K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 199K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 199K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 199K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.





