Đề thi thử tốt nghiệp THPT môn Hóa Liên trường Nghê An - Lần 2 năm 2025 có đáp án
55 người thi tuần này 4.6 3.7 K lượt thi 40 câu hỏi 60 phút
🔥 Đề thi HOT:
Đề thi thử THPTQG 2019 môn Hóa học cực hay có lời giải chi tiết (P1)
Đề Ôn thi THPTQG 2019 Hóa Học cơ bản, nâng cao có lời giải chi tiết (P1)
Tổng hợp đề thi Thử Hóa học cực hay có lời giải (Đề số 1)
Đề thi thử Hóa học cực hay có lời giải chi tiết (đề số 1)
Tổng hợp minh họa THPTQG 2019 Hóa Học có lời giải (Đề số 1)
Tổng hợp đề thi thử THPTQG 2019 - chuẩn cấu trúc của bộ giáo dục (Đề số 1)
Bộ đề tăng tốc luyện thi Hóa Học cực hay có lời giải chi tiết (đề số 1)
15 Đề thi thử THPTQG 2019 Hóa Học chuẩn cấu trúc của bộ giáo dục (Đề số 1)
Nội dung liên quan:
Danh sách câu hỏi:
Câu 1
Lời giải
C
Số C = 282.63,83%/12 = 15
Số O = 282.28,37%/16 = 5
Số H = (282 – 15.12 – 5.16)/1 = 22
Công thức phân tử của X là C15H22O5.
Câu 2
Lời giải
B
Dãy gồm các kim loại đều phản ứng với nước ở nhiệt độ thường tạo thành dung dịch có môi trường kiềm là Na, Ba, K.
Các dãy còn lại có Cr, Fe, Ni không phản ứng với nước ở nhiệt độ thường.
Câu 3
Lời giải
A
X2- tạo ra do X nhận thêm 2 electron → Cấu hình của X là: 1s22s22p4
X có 8e → X là O (Z = 8).
Câu 4
Lời giải
C
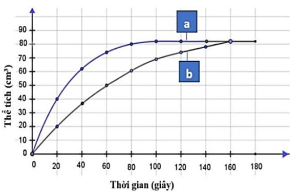
Thí nghiệm 2 dùng bột đá dạng mịn hơn thí nghiệm 1 nên tốc độ thoát khí sẽ nhanh hơn.
A. Đúng, tốc độ phản ứng trung bình trong 80 giây đầu tiên của thí nghiệm 1 và 2 lần lượt là 60/80 = 0,75 (cm³/s) và 80/80 = 1(cm³/s).
B. Đúng
C. Sai
D. Đúng, từ sau giây thứ 160 phản ứng 2 thí nghiệm đã dừng lại nên lượng khí thoát ra ở cả hai thí nghiệm không thay đổi.
Câu 5
Lời giải
A
Các biện pháp làm cân bằng chuyển dịch sang chiều thuận sẽ làm tăng hiệu suất tổng hợp NH3.
A. Tăng áp suất làm cân bằng chuyển dịch sang chiều thuận vì chiều thuận có số phân tử khí giảm.
B. Tăng nhiệt độ làm cân bằng chuyển dịch sang chiều nghịch vì chiều nghịch thu nhiệt.
C. Giảm nồng độ khí N2 làm cân bằng chuyển dịch sang chiều nghịch vì chiều nghịch tạo ra N2.
D. Giảm áp suất làm cân bằng chuyển dịch sang chiều nghịch vì chiều nghịch có số phân tử khí tăng.
Câu 6
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 199K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 7
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 199K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 8
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 199K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 9
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 199K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 199K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 11
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 199K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 199K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 13
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 199K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 14
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 199K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 199K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 16
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 199K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 199K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 199K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 199K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 199K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 199K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 199K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Đoạn văn 1
Dựa vào thông tin dưới đây để trả lời các câu hỏi từ câu 17 - 18:
Cho bảng giá trị thế điện cực chuẩn của các cặp oxi hóa - khử như sau:
|
Cặp |
Al3+/Al |
Zn2+/Zn |
Fe2+/Fe |
Cu2+/Cu |
Ag+/Ag |
|
E° (V) |
-1,676 |
-0,763 |
-0,440 |
0,340 |
0,799 |
Câu 23
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 199K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Câu 24
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 199K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Đoạn văn 2
PHẦN II. Câu trắc nghiệm đúng sai. Thí sinh trả lời từ câu 19 đến câu 22. Trong mỗi ý a), b), c), d) ở mỗi câu, thi sinh chọn đúng hoặc sai.
Vôi sống (CaO) có nhiều ứng dụng như: sản xuất vật liệu xây dựng, vật liệu chịu nhiệt, khử chua đất trồng, tẩy uế, sát trùng, xử lí nước thải,. Tuy nhiên, các lò nung vôi thủ công hoạt động tự phát có thể gây ô nhiễm môi trường. Ở các lò nung vôi công nghiệp, quy trình kiểm soát phát thải được thực hiện chặt chẽ hơn. Khảo sát một lò nung vôi công nghiệp sử dụng than đá làm nhiên liệu, giả thiết :
- Đá vôi chỉ chứa CaCO3 và cần cung cấp một nhiệt lượng 1800 kJ để phân hủy 1 kg đá vôi.
- Đốt cháy 1 kg than đá giải phóng một nhiệt lượng là 27000 kJ, trong đó 50% lượng nhiệt này được hấp thụ để phân hủy đá vôi.
- Than đá chứa 1% sulfur (ở dạng vô cơ và hữu cơ như FeS2, CaSO4, CxHySH,…) về khối lượng, 80% lượng sulfur bị đốt cháy tạo thành SO2 và 1,6% SO2 sinh ra phát thải vào khí quyển.
- Lò có công suất 420 tấn CaO/ngày.
Nhóm nghiên cứu đã đưa ra các kết luận :
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 199K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 199K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 199K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 199K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Đoạn văn 3
Ngô và mía là hai nguyên liệu chính được sử dụng trong sản xuất ethanol. Tuy nhiên, chúng là những loại cây lương thực quan trọng. Trong khi đó, cellulose – một nguồn nguyên liệu dồi dào và dễ tìm - cũng có thể dùng để sản xuất ethanol. Tuy giá thành sản xuất ethanol từ cellulose còn cao, do quá trình nuôi cấy nấm sản sinh enzyme cellulase để thuỷ phân cellulose thành glucose tốn kém nhiều năng lượng, nhưng đây vẫn là một hướng đi đầy hứa hẹn trong tương lai.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 199K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 199K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 199K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 199K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Đoạn văn 4
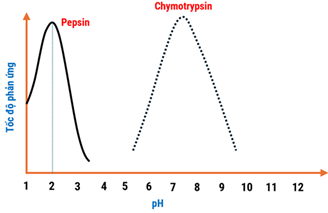
Hoạt tính xúc tác của enzyme càng cao, tốc độ thủy phân protein càng lớn. Hoạt tính enzyme phụ thuộc vào các yếu tố như nhiệt độ, pH,. Một nhóm học sinh đã khảo sát ảnh hưởng của pH đến hoạt tính của enzyme tiêu hoá protein ở người. Nhóm tiến hành thí nghiệm thuỷ phân albumin (protein có trong lòng trắng trứng) bằng enzyme pepsin ở nhiệt độ không đổi nhưng thay đổi pH của môi trường. Kết quả thu được như sau :
|
Ống nghiệm |
Thành phần |
Thời điểm t = 0 (phút) |
Thời điểm t = 20 (phút) |
|
1 |
Albumin + Pepsin + HCl 0,01M |
Đục |
Trong |
|
2 |
Albumin + Pepsin + H2O |
Đục |
Đục |
|
3 |
Albumin + Pepsin + NaHCO3 0,01M |
Đục |
Đục |
Sau đó, nhóm học sinh tiến hành thí nghiệm tương tự với enzyme chymotrypsin, thu được đồ thị như hình bên. Từ kết quả thí nghiệm, nhóm học sinh đã đưa ra các nhận định sau:
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 199K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 199K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 199K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 199K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Đoạn văn 5
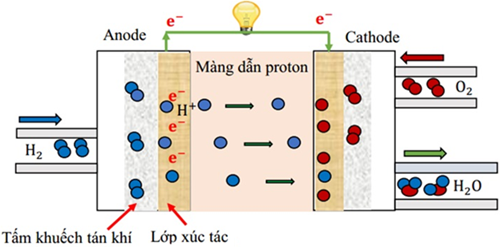
Pin nhiên liệu hydrogen là một nguồn sản xuất điện sạch với hiệu suất cao. Pin hoạt động thông qua phản ứng điện hoá giữa nhiên liệu là hydrogen và chất oxi hoá là oxygen. Khi pin hoạt động, hydrogen có vai trò tương tự như kim loại mạnh hơn trong pin Galvani; ở cathode, oxygen nhận electron và kết hợp với ion H+ để tạo thành nước. Dòng electron di chuyển qua mạch ngoài tạo ra dòng điện, cung cấp năng lượng cho các thiết bị hoặc động cơ.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 199K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 199K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 199K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.
Lời giải
Bạn cần đăng ký gói VIP ( giá chỉ từ 199K ) để làm bài, xem đáp án và lời giải chi tiết không giới hạn.